-




IL-17A+F Rationale
BIMZELX® bei PSO + PsA
nach 1 JahrBIMZELX® Gepoolte
3 JahresdatenBIMZELX® im Überblick
Referenzen und FKI
Nagel PSO
▼ D ieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnis-se über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung zu melden. Hinweise zur Meldung von Nebenwirkungen an das Bundesamt für Sicherheit im Gesundheitswesen: Traisengasse 5, 1200 WIEN, Fax: + 43 (0) 50 555 36207, Website: http://www.basg.gv.at/
AT-BK-2400039 (04/2024)
v2.0
Schnelle und anhaltende,
duale IL-17A- und IL-17F-Wirksamkeit
bei NagelpsoriasisBIMZELX®
START
oder unten Thema wählen
-






IL-17A+F Rationale
BIMZELX® bei PSO + PsA
nach 1 JahrBIMZELX® Gepoolte
3 JahresdatenBIMZELX® im Überblick
Referenzen und FKI
Nagel PSO
PSO Begleiterscheinungen können Patienten sehr belasten –
vor allem, wenn die sogenannten High Impact Areas betroffen sind.Nagel-Psoriasis bedeutet für Patienten nicht nur physische
Einschränkungen, sondern auch erheblichen emotionalen StressDie Auswirkungen der Nagel-PSO
auf die Patienten:• Starke Schmerzen und Behinderung bei der Ausübung von Arbeiten des täglichen Lebens1
• Eingeschränkte Selbstsicherheit
und Depression, denn die Erkrankung ist für viele sichtbar1• Erhöhtes Risiko Psoriasis Arthritis
zu entwickleln2Die Wirksamkeit von Therapien auf die Nägel ist daher
von wesentlicher Bedeutung, um das Leben und die
Aussichten der Patienten zu verbessern.der PSO Patienten
sind von
Nagel-Psoriasis
betroffen123-27%


-



IL-17 A/A,
IL-17 A/F,
IL-17 F/FIL-17 RA/RC
Rezeptor
der ZellenEntzündung
IL-23-abhängig
IL-23-unabhängig

BIMZELX® bei PSO + PsA
nach 1 JahrBIMZELX® Gepoolte
3 JahresdatenBIMZELX® im Überblick
Referenzen und FKI
Nagel PSO
IL-17A+F Rationale
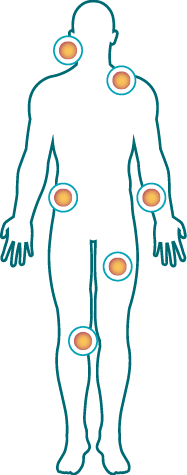
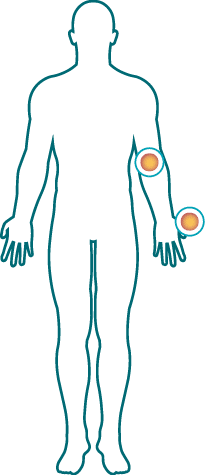
IL-17 Inhibitoren sind effektiv bei der Behandlung von
Nagel-Psoriasis – sowohl bei Patienten mit Plaque Psoriasis,
als auch bei Patienten mit Psoriasis Arthritis.Modifiziert nach Oliver et al.6

Patient mit PSO
Patient mit PsA
Immunvermittelte Entzündung bei
PSO, PsA und axSpA3-6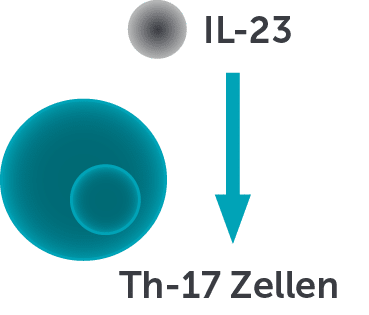


-


PSO






IL-17A+F Rationale
BIMZELX® Gepoolte
3 JahresdatenBIMZELX® im Überblick
Referenzen und FKI
Nagel PSO
BIMZELX® bei PSO + PsA
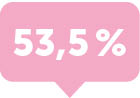
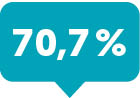
nach 1 JahrUnter Bimzelx® konnte bei 7 von 10 PSO-Patienten
eine vollständige Auflösung der Nagel-Psoriasis innerhalb
eines Jahres erzielt werden.1,2,7-9mNAPSI Definition >
PsA >
mNAPSI = 0
Baseline
mNAPSI > 10Bimekizumab 320 mg Q4W/Q8W (N=116)
Secukinumab 300 mg (N=99)
BE RADIANT7 (NRI) Woche 48
Baseline mNAPSI > 10 (NRI)Ansprechraten (%) mNAPSI = 0
0
20
40
60
80
100


-


PsA
PSO

TNFi-vortherapierte Patienten
Biologika-naive Patienten





IL-17A+F Rationale
BIMZELX® Gepoolte
3 JahresdatenBIMZELX® im Überblick
Referenzen und FKI
Nagel PSO
BIMZELX® bei PSO + PsA
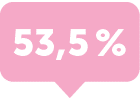
nach 1 JahrMit Bimzelx® konnte ebenso bei fast 7 von 10 PsA-Patienten
eine vollständige Auflösung der Nagel-Psoriasis innerhalb eines Jahres erzielt werden.7-9mNAPSI Definition >
BE RADIANT7 (NRI) Woche 48
Baseline mNAPSI > 10 (NRI)BE OPTIMAL8 und BE COMPLETE9 Woche 52
Baseline mNAPSI > 10 (NRI)Ansprechraten (%) mNAPSI = 0
Ansprechraten (%) mNAPSI = 0
0
0
20
20
40
40
60
60
80
80
100
100
BE OPTIMAL Bimekizumab 160 mg Q4W (N=217)
BE COMPLETE Bimekizumab 160 mg Q4W (N=159)
Bimekizumab 320 mg Q4W/Q8W (N=116)
Secukinumab 300 mg (N=99)
mNAPSI = 0
Baseline
mNAPSI > 10





-


Baseline
mNAPSI = 22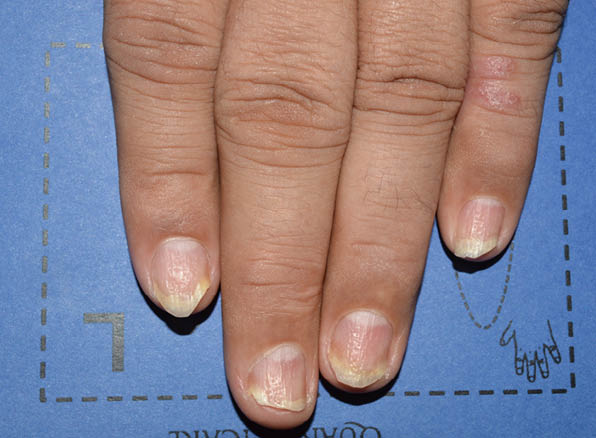
Woche 52
mNAPSI = 0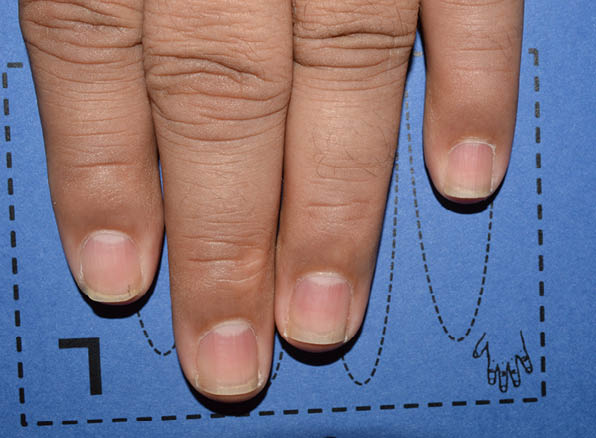
IL-17A+F Rationale
BIMZELX® Gepoolte
3 JahresdatenBIMZELX® im Überblick
Referenzen und FKI
Nagel PSO
BIMZELX® bei PSO + PsA
nach 1 JahrIn der BE VIVID Studie erreichten 18,6% der mit Bimzelx® 320 mg Q4W
behandelten Patienten nach 16 Wochen einen mNAPSI=010So kann es in der Praxis aussehen
BIMZELX® Patientenfall von Baseline bis Woche 52
BE VIVID Studienpatient (44 Jahre, männlich)10Bimzelx® Dosierung 320 mg Q4W
Der Patient hat der Nutzung
der Fotos zu werblichen
Zwecken zugestimmt.
Individuelle Ergebnisse
können abweichen.

-


Gepoolte Daten*: Ansprechraten (%) mNAPSI = 0
Baseline mNAPSI > 10 (mNRI)11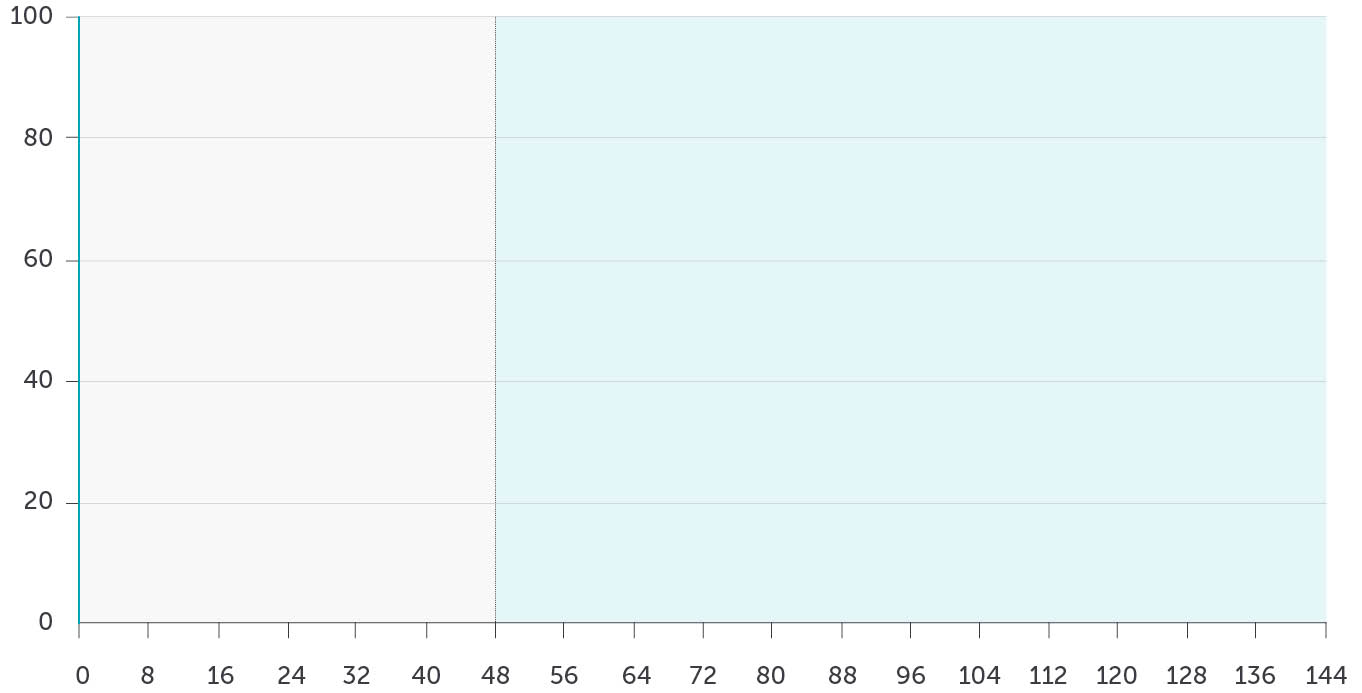






IL-17A+F Rationale
BIMZELX® bei PSO + PsA
nach 1 JahrBIMZELX® im Überblick
Referenzen und FKI
Nagel PSO
BIMZELX® Gepoolte
3 JahresdatenBis zu 3 Jahre anhaltende Wirksamkeit
für Patienten mit Nagel-Psoriasis11mNAPSI Definition >
* Gepoolte Daten: BE VIVID/BE READY/BE SURE (52/56/56 Wochen) Studien und 96 Wochen der Open-label Extension (OLE) Studie BE BRIGHT,
sowie 144 Wochen der BE RADIANT Phase 3b Studie. Die Analyse berücksichtigt nur Patienten, die initial auf Bimekizumab eingestellt wurden.Bei 7 von 10 Patienten
konnte nach
1 Jahr eine vollständige Remission der Nagel-Psoriasis erreicht und über 3 Jahre aufrecht erhalten werden.Wochen

BKZ Q4W/Q8W (mNRI; N=129)




-


• Tiefes Ansprechen bei mittelschwerer
bis schwerer Plaque-Psoriasis, aktiver
Psoriasis-Arthritis und mittelschwerer bis
schwerer Hidradenitis suppurativa12• Schnelle und anhaltende, duale Wirksamkeit
– auf Haut und Gelenke12• Indikationsspezifische Dosierungen12

© UCB Pharma GmbH, 2024. Alle Rechte vorbehalten. AT-BK-2400039 (04/2024)
IL-17A+F Rationale
BIMZELX® bei PSO + PsA
nach 1 JahrBIMZELX® Gepoolte
3 JahresdatenReferenzen und FKI
Nagel PSO
BIMZELX® im Überblick
BIMZELX® - Erwarten Sie mehr mit der selektiven,
dualen Hemmung von IL-17A und IL-17F bei
PSO, PsA und HS

-
Referenzen & Fachkurzinformation
Abkürzungen:
BKZ: Bimekizumab; HS: Hidradenitis suppurativa; IL: Interkeukin; mNAPSI: modified Nail Psoriasis Severity Index; mNRI: modifiied Non Responder Imputation; NRI: Non Responder Imputation; PsA: Psoriasis Arthritis; PSO: Plaque Psoriasis; Q4W: alle 4 Wochen; Q4/8W: alle 4/8 Wochen;
Referenzen:1. Merola JF et al. Dermatol Ther 2018; 31:e12589. 2. Gottlieb AB et al. J Dermatolog Treat 2022; 33(4):1907–1915. 3. Oliver R et al. BJD 2022; 186:652-663. 4. Adams R et al. Front. Immunol 2020; 11:1894. 5. Glatt S et al. Ann Rheum Dis 2018; 77:523–532. 6. van Baarsen L et al. Arthritis Research & Therapy 2014; 16:426. 7. Eyerich K et al. JAAD 2023; 89(3) Supplement AB 22. 8. Ritchlin CT et al. Ann Rheum Dis 2023; 82:1404–1414. 9. Coates LC et al. RMD Open 2024; 10:e003855. 10. Papp K et al. SKIN The Journal of Cutaneous Medicine 2022; 5(1):p18. 11. Merola J.F. et al. SKIN The Journal of Cutaneous Medicine; 8(1): p304. 12. Fachinformation BIMZELX®; Stand April 2024.
Fachkurzinformation: Bimzelx 160 mg Injektionslösung in einer Fertigspritze, Bimzelx 160 mg Injektionslösung im Fertigpen▼ Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung zu melden. Hinweise zur Meldung von Nebenwirkungen an das Bundesamt für Sicherheit im Gesundheitswesen: Traisengasse 5, 1200 WIEN, Fax: + 43 (0) 50 555 36207, Website: http://www.basg.gv.at/
Zusammensetzung: Jede Fertigspritze/jeder Fertigpen enthält 160 mg Bimekizumab in 1 ml Lösung. Bimekizumab ist ein humanisierter monoklonaler IgG1-Antikörper, hergestellt mittels rekombinanter DNA-Technologie in gentechnisch modifizierten Ovarialzellen des chinesischen Hamsters (CHO-Zelllinie).Sonstige Bestandteile: Glycin, Natriumacetat-Trihydrat, Essigsäure 99 %, Polysorbat 80, Wasser für Injektionszwecke.
Anwendungsgebiete: Plaque-Psoriasis: Bimzelx wird angewendet zur Behandlung erwachsener Patienten mit mittelschwerer bis schwerer Plaque-Psoriasis, die für eine systemische Therapie infrage kommen. Psoriasis-Arthritis: Bimzelx wird allein oder in Kombination mit Methotrexat zur Behandlung erwachsener Patienten mit aktiver Psoriasis-Arthritis angewendet, die auf ein oder mehrere krankheitsmodifizierende Antirheumatika (disease-modifying antirheumatic drugs, DMARDs) unzureichend angesprochen oder diese nicht vertragen haben. Axiale Spondyloarthritis: Nicht-röntgenologische axiale Spondyloarthritis (nr-axSpA): Bimzelx wird angewendet zur Behandlung erwachsener Patienten mit aktiver nicht-röntgenologischer axialer Spondyloarthritis mit objektiven Anzeichen einer Entzündung, nachgewiesen durch erhöhtes C-reaktives Protein (CRP) und/oder Magnetresonanztomographie (MRT), die auf nicht-steroidale Antirheumatika (NSARs oder non-steroidal anti-inflammatory drugs, NSAIDs) unzureichend angesprochen oder diese nicht vertragen haben. Ankylosierende Spondylitis (AS, röntgenologische axiale Spondyloarthritis): Bimzelx wird angewendet zur Behandlung erwachsener Patienten mit aktiver ankylosierender Spondylitis (AS), die auf eine konventionelle Therapie unzureichend angesprochen oder diese nicht vertragen haben. Hidradenitis suppurativa (HS): Bimzelx wird angewendet zur Behandlung erwachsener Patienten mit aktiver mittelschwerer bis schwerer Hidradenitis suppurativa (Acne inversa), die auf eine konventionelle systemische HS Therapie unzureichend angesprochen haben (siehe Abschnitt 5.1 der Fachinformation).
Gegenanzeigen: Überempfindlichkeit gegen den Wirkstoff oder einen der in Fachinformation Abschnitt 6.1 genannten sonstigen Bestandteile. Klinisch relevante aktive Infektionen (z.B. aktive Tuberkulose, siehe Abschnitt 4.4 der Fachinformation).
Inhaber der Zulassung: UCB Pharma S.A., Allée de la Recherche 60, B-1070 Bruxelles, Belgien.
Rezeptpflicht/Apothekenpflicht: rezept- und apothekenpflichtig, wiederholte Abgabe verboten.
ATC-Code: L04AC21
Weitere Angaben zu Dosierung, Nebenwirkungen, Wechselwirkungen, Anwendung in der Schwangerschaft und Stillzeit, Gewöhnungseffekten und besonderen Warnhinweisen und Vorsichtsmaßnahmen für die Anwendung entnehmen Sie bitte der veröffentlichten Fachinformation.
Stand der Information: 04/2024.
© UCB Pharma GmbH, 2024. Alle Rechte vorbehalten. AT-BK-2400039 (04/2024)
-
mNAPSI Def inition11
0
13
3
3
3
1
1
1
1
Oncholyse
teilweise oder
vollständige
Ablösung des
Nagels vom
NagelbettCrumbling –
Krümelnägelvollständige
Zerstörung der
NagelplattePitting -
Tüpfelnägel:punktförmige
Einsenkungen auf der
NagelplatteLeukonychie – Ölflecknagel
gelb-braune
Verfärbung
unter dem
NagelNagelbett
HyperkeratoseSplitterblutungen
strichförmigeVerfärbungen
durch kleine
BlutungenRote Flecken
in LunulaScoreberechnung
Score 0 = freier Nagel
Score pro Nagel 0-13
Maximalscore von 130



Downloading for offline webApp usage - please wait...